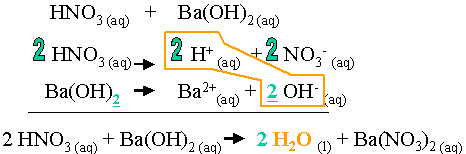
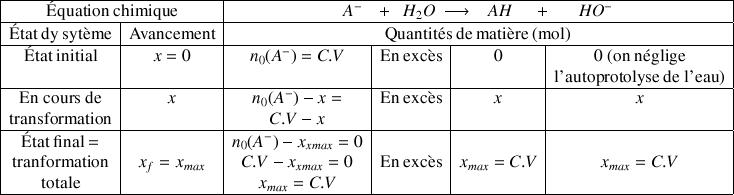G) Sels Dans le chapitre 1, Acide + Base Sel + Eau HCl(aq) + NaOH(aq) NaCl(aq) + H2O Les sels sont des électrolytes forts qui se dissocient entièrement. - ppt video online télécharger

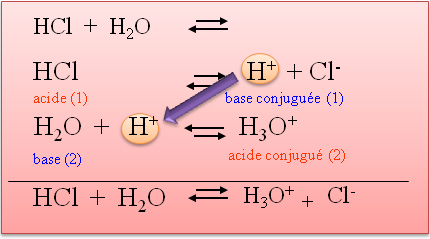
Déterminer la composition d'un système par des méthodes physiques et chimiques – Physique-Chimie Franco
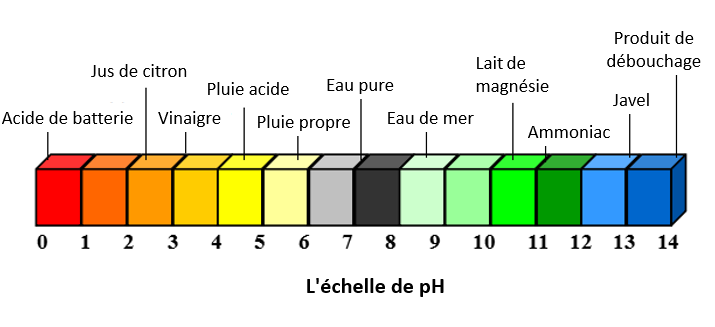
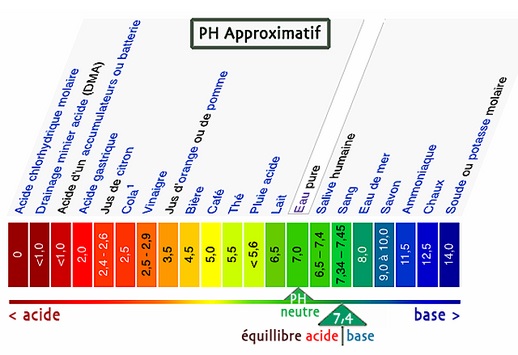
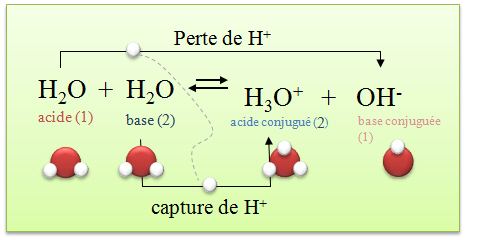
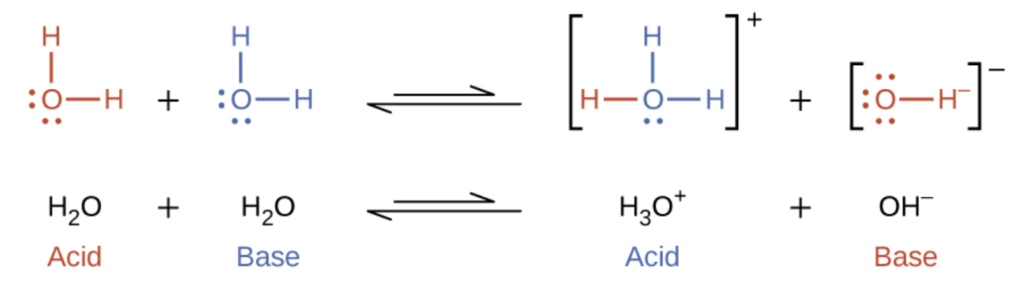
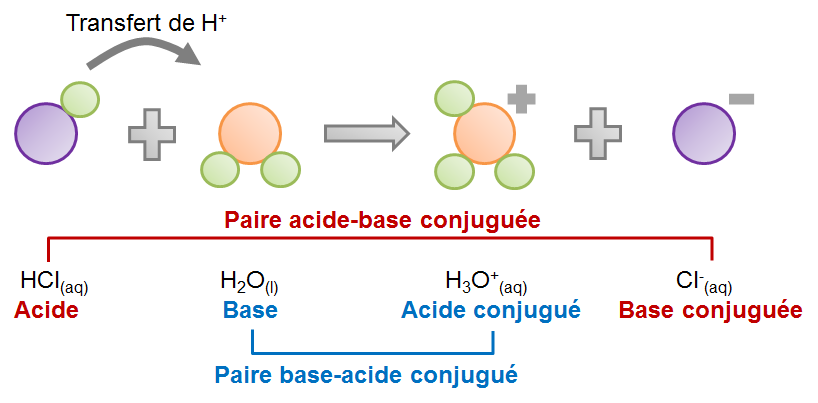
LES REACTIONS ACIDE-BASE 1. Le pH 1.1 Définition Le pH (potentiel hydrogène) est une grandeur qui donne une information sur la

G) Sels Dans le chapitre 1, Acide + Base Sel + Eau HCl(aq) + NaOH(aq) NaCl(aq) + H2O Les sels sont des électrolytes forts qui se dissocient entièrement. - ppt video online télécharger